Brustkrebs: Alles, was Sie wissen müssen
Worum handelt es sich bei Brustkrebs?
Definition
Die Brust (auch Brustdrüse genannt) besteht aus verschiedenen Kompartimenten, und zwar aus:
- Läppchen, in denen die Milchsynthese stattfindet;
- und den Milchgängen, die die Milch sammeln und zur Brustwarze leiten.
Diese Kompartimente sind von Stützgewebe umgeben, das aus Fett, Fasern sowie Blut- und Lymphgefäßen besteht.
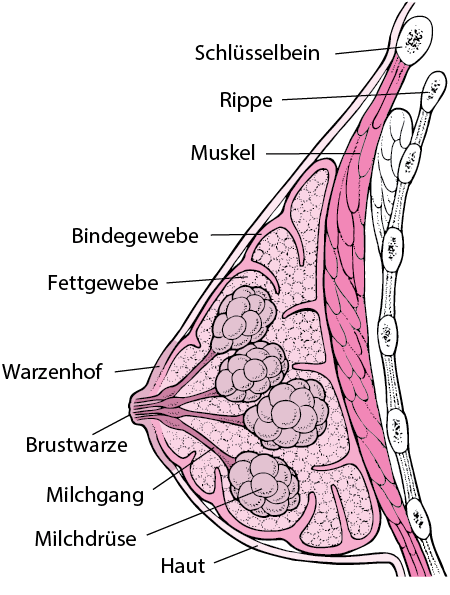
Quelle: MSD Manual
Brustkrebs ist die häufigste und tödlichste Krebsart bei Frauen in Deutschland. Er entsteht durch eine Störung der Zellen, die sich vermehren und normalerweise eine Masse bilden, die als Tumor bezeichnet wird.
Es gibt verschiedene Entwicklungsstadien der Krankheit:
- Unter den gutartigen Tumoren (Adenofibrome genannt) finden sich:
- Adenofibrom oder Fibroadenom: Es handelt sich um einen Tumor, der aus Faser- und Drüsengewebe besteht; er ist bei einer Mammographie und im Ultraschall gut zu erkennen. Er verursacht nie eine axilläre Adenopathie und erfordert eine Überwachung oder Operation, wenn die Masse größer als 30 mm ist.
- Fibrozystische Erkrankung: Diese entspricht einer oder mehreren verkalkten Zysten und erfordert eine Operation.
- Bei den lokalisierten Krebsarten (im Bereich der Gänge und Läppchen, ohne Lymphknotenbefall), die den Stadien 0 bis II entsprechen, werden unterschieden:
- Carcinoma in situ: duktales oder lobuläres Karzinom (4% bzw. 2,5% der Brustkrebsfälle), ohne dass die Basalmembran überschritten wird. Bei der Mammographie entdeckt und durch eine Biopsie bestätigt, besteht ein Risiko von 33%, in den nächsten 10 Jahren ein invasives Karzinom zu entwickeln.
- Invasives Karzinom: duktales oder lobuläres Karzinom (75% bzw. 13% der Brustkrebsfälle) mit invasiver Beteiligung des umliegenden Gewebes. Zwei Drittel der Krebserkrankungen werden in diesem Stadium durch eine Mammographie entdeckt.
- Der Krebs ist lokal fortgeschritten (Stadium III), wenn die Krebszellen bis zu den axillären Lymphknoten oder zu den inneren Lymphknoten der Brust in der Brustwand fortgeschritten sind
- Der Krebs gilt als metastasiert (Stadium IV), wenn die Krebszellen die Brust befallen haben und in die umliegenden Lymph- oder Blutgefäße eingedrungen sind. Die wichtigsten Metastasierungsorte sind: Knochen (50%), lokoregionär (40%), Leber (30%), Lunge oder Pleura (20%) und Gehirn (10%).
Die meisten Brustkrebsfälle sind hormonabhängig, von Östrogen gesteuert (ER-positiv). Einige sind von der Überexpression von HER2 (Human Epidermal Growth Factor Receptor 2) abhängig, einem Transmembranrezeptor, der an der Regulierung der Zellproliferation beteiligt ist. Die anderen sind so genannte dreifach negative, da ER und HER2 negativ sind und es keine charakteristischen Oberflächenmarker gibt.
Kommt Brustkrebs häufig vor?
Mit 67 000 Neuerkrankungen pro Jahr handelt es sich um die häufigste Krebserkrankung bei Frauen. Er betrifft 1 von 8 Frauen und hat ein Geschlechterverhältnis Frau/Mann von 99 (Brustkrebs gibt es auch bei Männern). Es handelt sich bei einem Auftreten vor dem 30. Lebensjahr um eine seltene Krebserkrankung, mit einem Höchstwert des Entstehens von Krebs zwischen dem 60. und 69. Lebensjahr. Die relative 5-Jahres-Überlebensrate liegt bei 87% und die relative 10-Jahres-Überlebensrate liegt bei 82% der lokalisierten Formen. Dennoch ist sie die häufigste Krebstodesursache bei Frauen mit einer Sterblichkeitsrate von 18 000 Todesfällen pro Jahr in Deutschland.
Symptome und Komplikationen bei Brustkrebs
Die Symptome von Brustkrebs sind die folgenden:
- Das Auftreten eines festen oder beweglichen Knotens (Kugel) in der Brust, oft mit unregelmäßigen Konturen, der bei der Selbstabtastung wahrgenommen wird
- Geschwollene und harte Lymphknoten in der Achselhöhle, die nicht schmerzhaft sind
- Eine Veränderung der Form der Brust
- Eine Veränderung des Aussehens der Haut der Brust (Rötung, Ödem oder ähnlich wie Orangenhaut) oder der Brustwarze oder des Brustwarzenhofs (Rückgang, Farbveränderung usw.)
- Seltener: spontaner Ausfluss aus einer Brustwarze
Wenn sich der Brustkrebs auf den Rest des Körpers ausgebreitet hat, können andere Symptome auftreten, wie Müdigkeit, Übelkeit, Gewichtsverlust, Knochenschmerzen oder Sehstörungen.
Ursachen und Risikofaktoren für Brustkrebs
Unter den Risikofaktoren für Brustkrebs finden sich auch individuelle Faktoren:
- Hormonelle Faktoren, die einem Hyperöstrogenismus entsprechen:
- Frühpubertät, vor dem 12. Lebensjahr
- Späte Menopause, nach dem 50. Lebensjahr
- Nullipara (Frauen, die noch nie ein Kind geboren haben): Das Risiko, an Brustkrebs zu erkranken, nimmt mit der Anzahl der Schwangerschaften ab und steigt mit dem späten Zeitpunkt einer ersten Schwangerschaft (> 35 Jahre)
- Hormonersatztherapie in den Wechseljahren seit mehr als 10 Jahren
- Fettleibigkeit nach der Menopause (Östrogen wird auch von Fettzellen produziert).
- Alter: Das Risiko, an Brustkrebs zu erkranken, ist im Alter zwischen 60 und 64 Jahren am höchsten
Es existieren auch familiäre oder genetische Risikofaktoren:
- Wenn mehrere Frauen in der Familie (ersten und zweiten Grades) Brustkrebs haben (oder hatten)
- Wenn eine Frau in der Familie vor dem 40. Lebensjahr an Brustkrebs erkrankt ist
- Wenn mehrere Personen in der Familie Darm- oder Eierstockkrebs haben (oder hatten)
Unter den genetischen Prädispositionen finden sich:
- Mutation der Prädispositionsgene BRCA1 und BRCA2, die bei 5 bis 7% der Brust- und/oder Eierstockkrebsfälle vorkommt
- Mutation anderer Gene (p53, PI3K, PALB2)
Schließlich gibt es noch verhaltensbedingte Risikofaktoren
- In Bezug auf die Ernährung (übermäßiger Konsum von tierischen Fetten, Zucker und Alkohol)
- Rauchen
Diagnose von Brustkrebs
Vorsorge
Die Selbstabtastung ist ein einfaches Verfahren, das von allen Frauen einmal im Monat durchgeführt werden sollte, und zwar immer zur gleichen Zeit, einige Tage nach Ende der Periode. Dies ermöglicht die frühzeitige Erkennung einer Anomalie und kann dem Hausarzt gemeldet werden. Dabei steht oder sitzt man vor einem Spiegel und begutachtet das Aussehen der Brüste (Flüssigkeitsaustritt aus der Brustwarze, Grübchen, Risse, Orangenhaut, …). Als Nächstes wird der Arm angehoben und die Brust gründlich sowie fest mit den drei Fingern der anderen Hand abgetastet, indem kleine Kreise von der Außenseite der Brust (es sollte besonders auf den Bereich zwischen Achselhöhle und Brust geachtet werden) bis zur Brustwarze (so wird geprüft, ob es Knoten oder Verhärtungen gibt) gezogen werden.
Die Mammographie ist die Standard-Röntgenuntersuchung, bilateral und vergleichend. Zu den Anzeichen, die auf Brustkrebs hindeuten, gehören Trübungen, Architekturstörungen oder Mikroverkalkungen.
Ab dem 30. Lebensjahr wird eine klinische Untersuchung der Brüste durch Abtasten durch einen Arzt empfohlen. Zwischen 50 und 69 Jahren, ohne Symptome oder andere Risikofaktoren außer dem Alter, wird eine Mammographie alle zwei Jahre empfohlen.
Die Ultraschall gilt als Zweitlinienuntersuchung zur Ergänzung der Mammographie, die durchgeführt wird, wenn die Brüste dicht (jung) sind, oder um eine bei der Mammographie festgestellte Anomalie zu charakterisieren.
Diagnostischer Ansatz
Die Diagnose Brustkrebs wird nach mehreren Schritten gestellt:
- Zunächst wird der Patient befragt, um verschiedene Risikofaktoren festzustellen
- Anschließend wird eine klinische Untersuchung durchgeführt, bei der durch Abtasten der Knoten nach einer axillären Lymphadenopathie gesucht wird
- Die Diagnose wird danach durch bildgebende Verfahren gestellt: Mammographie, Ultraschall der beiden Brüste sowie Lymphknoten, MRT, PET (Positronen-Emissions-Tomographie), PET-CT
- Schließlich werden Biopsien unter Mammographie- oder Ultraschallkontrolle durchgeführt, um eine histologische Diagnose zu stellen, die die einzige Möglichkeit ist, die Prognose und die in Frage kommende Behandlung zu beurteilen
Bei lokalisiertem, infiltrierendem Krebs können weitere Untersuchungen durchgeführt werden: bilaterale Mammographie, Leberultraschall, Bauch- und Becken-CT, Röntgenaufnahme des Brustkorbs, Knochenszintigraphie, MRT und Gehirn-CT (bei neurologischen Symptomen) oder auch ein FDG-PET/CT.
TNM-Klassifikation
Diese Klassifikation ist für die Wahl der therapeutischen Strategie erforderlich.
- T = Größe:
- T1: wenn der Tumor < 2 cm ist
- T2: wenn der Tumor an der Stelle der breitesten Ausdehnung zwischen 2 und 5 cm groß ist (ab T2 ist eine Histologie (Gewebeanalyse) für die Entscheidung bzgl. der Behandlung notwendig)
- T3: wenn die größte Ausdehnung des Tumors > 5 cm beträgt
- T4: wenn sich der Tumor unabhängig von seiner Größe direkt auf die Brustwand T4a oder die Haut T4b ausdehnt
- T4d: Es handelt sich um ein entzündliches Karzinom
- N = regionale Lymphknoten (Node auf Englisch)
- Nx: Wenn es keine Informationen zu den Lymphknoten gibt
- N0: Wenn es keine Anzeichen für einen Lymphknotenbefall gibt
- N1: wenn eine mobile, homolaterale axilläre Lymphadenopathie beobachtet werden kann (Befall von ein bis drei Lymphknoten)
- N2: wenn axilläre Lymphadenopathien (N2a) (vier bis neun Lymphknoten) oder homolaterale Brustadenopathien (N2b) beobachtet werden, die fixiert oder induriert sein können
- N3a: wenn homolaterale subklavikuläre Lymphadenopathien mit axillären Lymphadenopathien ( mehr als zehn Lymphknoten) vorhanden sind
- N3b: wenn homolare Lymphadenopathien der Brustarterie mit axillären Lymphadenopathien beobachtet werden
- N3c: wenn Lymphadenopathien oberhalb des Schlüsselbeins beobachtet werden
- M = Metastasen:
- M0: Wenn es keine Metastasen gibt
- M1: Wenn Metastasen beobachtet werden
Pathologische Untersuchung
Das von Elston und Ellis modifizierte Bloom-Richardson-Grading: BRE-Graduierung
Der Aggressivitäts-Score wird anhand von drei Kriterien aufgestellt:
- Anteil der tubulären Strukturen des Tumors
- Ausmaß der Kernpolymorphien
- Anzahl der Mitosen
Man bewertet somit:
- Den histologischen Aspekt: > 75% des Gewebes (1), 10-75% des Gewebes (2), <10% des Gewebes (3)
- Die Kernpolymorphien: Gering (1), mittelgradig (2), hochgradig (3)
- Die Anzahl der Mitosen: ≤1 / Hauptgesichtsfeld (1), 2 / Hauptgesichtsfeld (2), ≥3 / Hauptgesichtsfeld (3)
Die Summe ergibt die BRE-Graduierung an:
- G1: Scores 3, 4 oder 5 für wenig aggressive Tumore
- G2: Scores 6 oder 7 für mäßig aggressive Tumore
- G3: Scores 8 oder 9 für aggressive Tumore
Charakteristische Tumormarker
Es gibt verschiedene charakteristische Marker für Brustkrebs:
- Hormonrezeptoren (HR oder ER) für Östrogen RO oder Progesteron RP können durch Immunhistochemie gemessen werden. Auf diese Weise lässt sich feststellen, ob eine Hormonabhängigkeit besteht oder nicht, wobei zu berücksichtigen ist, dass ein ER-positiver Brustkrebs weniger aggressiv ist
- Das HER2-Onkogen (Erb-B2) codiert für den EGFR-Rezeptor 2 (HER2), dessen Überexpression das Zellwachstum stimuliert. Eine Überexpression dieses Onkogens wird bei 30 % der metastasierenden Brustkrebsfälle beobachtet und dreifach positive HER2-Brustkrebsfälle sind sehr aggressiv
- Der Prozentsatz der Zellen in der S-Phase (DNA-Replikationsphase) kann mittels Durchflusszytometrie berechnet werden
- Der Ki-67-Labeling-Index schließlich ist ein prognostischer Wert (progressionsfreies Überleben und Gesamtüberleben), wobei Ki ein Zellproliferationsgen ist.
Behandlung von Brustkrebs
Operation
Eine Operation ermöglicht die Entfernung des Tumors, aber auch die Bestätigung der Diagnose und die Bestimmung des Entwicklungsstadiums durch die Untersuchung des Befalls der axillären Lymphknoten.
Durchgeführt werden kann:
- Eine Lumpektomie, d.h. eine konservative Operation, die durchgeführt wird, wenn der Tumor gut lokalisiert und kleiner als 3 cm groß ist (ohne ästhetische Folgen)
- Eine totale Mastektomie (1/3 der Fälle), wenn der Tumor groß und multifokal ist oder wenn es nach einer konservativen Behandlung zu einem Rückfall kommt
Bei Frauen mit BRCA1/2-Mutation ist die prophylaktische beidseitige Mastektomie trotz ihres eingreifenden Charakters die wirksamste Maßnahme zur Verringerung des Krebsrisikos.
Die Suche nach dem „Sentinel-Lymphknoten“ ermöglicht es außerdem, bei kleinen Tumoren nur bestimmte Lymphknoten zu entfernen (die Lymphknoten, die an erster Stelle im Abflussgebiet des Tumors liegen). Sie werden durch Injektion von Farbstoff (Patentblau) in der Nähe des Tumors lokalisiert. Der Lymphknoten wird intraoperativ untersucht:
- Bei negativem Befund (kein Befall mit Krebszellen): Es wird keine axilläre Kuration durchgeführt, und es gibt daher weniger Komplikationen
- Bei positivem Befund: acht bis zehn Lymphknoten werden entfernt
Schließlich wird eine sofortige Rekonstruktion nach einer Mastektomie nicht empfohlen, wenn eine Strahlentherapie geplant ist.
Strahlentherapie
Wenn eine Strahlentherapie vier Wochen nach der Operation durchgeführt wird, wird sie als „adjuvant“ bezeichnet. Ihr Ziel ist es, das Risiko von lokalen Rezidiven der Erkrankung so weit wie möglich zu verringern und das Gesamtüberleben zu verlängern. Vier Bereiche können durch Strahlentherapie behandelt werden:
- Die Brustdrüse nach einer Lumpektomie
- Das Tumorbett (d.h. der Bereich der Brust, in dem sich der Tumor vor der Operation befand)
- Die Brustwand nach einer Mastektomie
- Die Lymphknotenbereiche in der Nähe des Tumors
Die Gesamtdosis beträgt 50 Gy, d.h. 2 Gy pro Tag, 5 Tage die Woche und das 5 Wochen lang.
Eine Strahlentherapie wird bei einem Rückfall nicht eingesetzt, wenn bereits beim ersten Mal eine Strahlentherapie durchgeführt wurde.
Mögliche Komplikationen sind Hautrötungen, Brustödeme, Schmerzen, Müdigkeit und langfristige kardiovaskuläre sowie pulmonale Probleme.
Systemische medikamentöse Behandlung
Es gibt drei Arten:
- Unter einer Hormontherapie versteht man die Ausschaltung von RH-positivem (ER-positivem) Krebs durch Hemmung der hormonellen Stimulation
- Eine Chemotherapie entspricht der Hemmung des Tumorwachstums durch konventionelle zytotoxische Chemotherapie
- Gezielte Therapien bestehen aus der Hemmung des Tumorwachstums durch Hemmung der Neovaskularisierung, der Wiederherstellung der Apoptose (programmierter Zelltod) oder der Stimulierung der Immunantwort des Patienten
Hormontherapie
Ziel ist es, das rezidivfreie Überleben und das Gesamtüberleben nach einer Operation und/oder Strahlentherapie zu verlängern.
Bei prämenopausalen Frauen kann die LH-Produktion durch LH-RH-Analoga wie Goserelin (Zoladex®) oder Leuprorelin (Enantone® LP) gehemmt werden, bei denen es sich um subkutan injizierte Implantate handelt, die über einen längeren Zeitraum (1 Monat) verabreicht werden. Sie sind indiziert bei HR-positivem (ER-positivem) und dreifach HER2-positivem Brustkrebs oder wenn eine gynäkologische Indikation mit Endometriose und Uterusmyomen vorliegt. Mögliche Nebenwirkungen sind Kopfschmerzen, Stimmungsschwankungen, Hitzewallungen, Schweißausbrüche, verminderte Libido, Gelenkschmerzen, Hautreaktionen, hoher Blutdruck oder Risiko von Brüchen.
Alternativ können konkurrierende Östradiol-Inhibitoren wie Tamoxifen (Nolvadex®) mit 20 mg pro Tag eingesetzt werden. Es ist indiziert bei Brustkrebsfällen von prämenopausalen Frauen, die RH-positiv (ER+) und HER2-negativ sind. Bei einer fünfjährigen Behandlung sinkt das Risiko eines erneuten Auftretens der Krankheit von 45 auf 8% und das Sterberisiko von 32 auf 10 %. Sofortige Unverträglichkeiten können beobachtet werden: Hitzewallungen, vaginaler Pruritus (Juckreiz), Leukorrhoe (blutloser Scheidenausfluss) und Übelkeit. Außerdem erhöht sich das Risiko von Thrombosen um etwa 1% (Schlaganfall, Embolie), für Gebärmutterkrebs um 0,4 bis 1,7% (gynäkologische Überwachung erforderlich) und für Katarakte. Es gibt auch Wechselwirkungen mit CYP2D6-Inhibitoren (Paroxetin, Fluoxetin, Chinidin sollten bei einer Behandlung mit Tamoxifen vermieden werden).
Darüber hinaus kann Fulvestrant (Faslodex®) auch als Zweitlinienbehandlung bei postmenopausalen Frauen eingesetzt werden.
Bei postmenopausalen Frauen werden Aromatasehemmer eingesetzt. Aromatase kommt in Tumorgewebe, Nebennieren, Muskeln, Fettgewebe, Leber (und in den Eierstöcken und Brüsten bei Frauen nach der Menopause) vor. Seine Hemmung führt zu einem Rückgang der Synthese von zirkulierenden Östrogenen und Östrogenrezeptoren (ER). Diese Aromatasehemmer können sein:
- Kompetitiv (Steroidal): Formestan (Lentaron®), Exemestan (Aromasin®)
- Nicht-kompetitiv (Nicht-steroidal): Letrozol (Femara®), Anastrozol (Arimidex®)
Sie werden alle oral eingenommen und sind für ER-positivem Brustkrebs bei postmenopausalen Frauen indiziert. Leichte bis mittelschwere Nebenwirkungen, die beobachtet werden können, sind Hitzewallungen, Haarausfall, Verdauungsstörungen, Asthenie, Schläfrigkeit, Kopfschmerzen oder Hautausschlag. Osteoartikuläre Schmerzen können ebenfalls beobachtet werden, und das Osteoporoserisiko ist im Vergleich zur Behandlung mit Tamoxifen erhöht.
Chemotherapie
Ihr Ziel ist es, das Tumorwachstum zu hemmen, indem sie in die Synthese der Nukleinsäuren (DNA und RNA) eingreift, die Zellteilung blockiert, die Neovaskularisierung des Tumors hemmt, die Apoptose (Selbstzerstörung der Zellen) auslöst oder wiederherstellt und die Immunantwort stimuliert.
Die verwendeten Moleküle haben alle eine Wirkung auf die DNA und können wie folgt sein:
- Antimetaboliten: 5-Fluorouracil (5-FU) oder Capecitabin
- Alkylierungsmittel: Cyclophosphamid (CPM)
- Mittel zur Interkalation oder Inhibitoren der Topoisomerasen 1 und 2: Anthracycline (Epirubicin, Doxorubicin).
Diese drei Moleküle werden im FEC-Schema (Fluorouracil, Epirubicin und Cyclophosphamid) kombiniert.
- Spindelgifte oder Antimitotika: Dazu gehören Polymerisationshemmer (Vinca-Alkaloide wie Vinblastin, Vincristin oder Vinorelbin) und Depolymerisationshemmer (Taxane wie Paclitaxel und Docetaxel).
Häufige Nebenwirkungen bei dieser Behandlungsform sind:
- Hämatologischer Art (Neutropenie, Thrombozytopenie, Anämie)
- Verdauungsstörungen (Übelkeit und Erbrechen)
- Stomatologischer Art (Stomatitis, Mukositis oder Entzündung der Schleimhäute)
- Dermatologischer Art (Alopezie oder Haarausfall)
- Gynäkologischer Art (Amenorrhoe oder Ausbleiben der Menstruation)
Einige Nebenwirkungen sind spezifisch:
- Mund- und Rachenschleimhautentzündung (Entzündungen, Brennen, Aphten und Mykosen) und Hand-Fuß-Syndrom bei 5-FU oder Capecitabin
- Urotoxizität (hämorrhagische Zystitis) bei Cyclophosphamiden
- Dosisabhängige Kardiotoxizität bei Epirubicin/Doxorubicin
- Haut-/Zungenödeme, Hautrötungen (Vorbeugung mit oralem Kortikosteroid am Vortag und für zwei Tage) bei Docetaxel
- Neuropathie und Myalgie (Vorbeugung mit oralem Steroid) bei Paclitaxel
- Neuropathien (Parästhesien) bei Vinorelbin
Molekulare Therapie
Verschiedene Moleküle können zum Einsatz kommen:
- Bevacizumab (Avastin®) ist ein monoklonaler Antikörper gegen VEGF-A, der für die Behandlung von metastasierendem Brustkrebs in Kombination mit Paclitaxel oder Capecitabin angezeigt ist. Es wird als intravenöse (IV) Injektion alle 2 bis 3 Wochen verabreicht. Nebenwirkungen, die beobachtet werden können, sind Bluthochdruck (Inzidenz von AH Grad III/IV ≃ 4%), Proteinurie (Vorhandensein von Eiweiß im Urin), erhöhte Inzidenz von arteriellen Thromboembolien ≃ 3,8%) oder Herzinsuffizienz.
- Trastuzumab (Herceptin®) ist ein HER2-blockierender monoklonaler Antikörper. Es bei Brustkrebs viele Indikationen: nicht metastasierend, nach Anwendung von oder in Kombination mit zytotoxischen Medikamenten (Taxane, Alkylierungsmittel wie Carboplatin) oder metastasierend in Kombination mit einem Taxan und Hormontherapie. Es kann intravenös oder subkutan injiziert werden. Als Nebenwirkungen können Dyspnoe oder Kardiomyopathie auftreten (vor Beginn der Behandlung ist ein Herzultraschall erforderlich), weshalb es nicht mit Anthrazyklinen kombiniert werden kann.
- Lapatinib (Tyverb®) ist ein EGFR-Tyrosinkinaseinhibitor (TKI). Es ist indiziert bei Brustkrebs mit HER2-Rezeptor-Überexpression in Kombination mit Capecitabin, Trastuzumab oder einem Aromatasehemmer, je nach Situation und vorheriger Behandlung. Es wird mündlich eingenommen. Zu den unerwünschten Wirkungen, die beobachtet werden können, gehören Durchfall, Hand-Fuß-Syndrom, Hautausschlag, Kardiotoxizität und Lungenerkrankungen (interstitielle Schäden und Pneumonitis).
Ebenfalls verwendet werden:
- Pertuzumab (Perjeta®), indiziert bei metastasiertem oder lokal rezidivierendem HER2-positivem Brustkrebs in Kombination mit Trastuzumab und Docetaxel bei Erwachsenen, die keine vorherige Anti-HER2-Therapie oder Chemotherapie für ihre metastasierte Erkrankung erhalten haben.
- T-DM1 (Trastuzumab-Emtansin) (Kadcyla®), ein ADC (Antikörper-Wirkstoff-Konjugat), ist indiziert für die Monotherapie von inoperablem, lokal fortgeschrittenem oder metastasiertem HER2-positivem Brustkrebs, der zuvor mit Trastuzumab und Taxan, einzeln oder in Kombination, behandelt wurde.
- Everolimus (Afinitor®), ein selektiver Hemmer von mTOR (einer Serin-Threonin-Kinase, deren Aktivität bekanntermaßen bei vielen menschlichen Krebsarten dereguliert ist), ist für die Behandlung von Hormonrezeptor-positivem, HER2-negativem fortgeschrittenem Brustkrebs in Kombination mit Exemestan bei postmenopausalen Frauen angezeigt.
- Schließlich CDK-Inhibitoren (Cyclin-abhängige Proteinkinasen, die für die Auslösung und Koordinierung der verschiedenen Phasen des Zellteilungszyklus verantwortlich sind). Dazu gehören Palbociclib (Ibrance®), Ribociclib (Kisqali®) und Abemaciclib (Verzenios®). Alle drei sind CDK 4/6-Inhibitoren, die bei metastasiertem HR-positivem, HER2-negativem Brustkrebs in Kombination mit Letrozol oder Fulvestrant eingesetzt werden.
Leben mit Brustkrebs
Medizinische Überwachung
Frauen, die wegen Brustkrebs behandelt wurden, müssen über mehrere Jahre hinweg engmaschig überwacht werden, um das Auftreten von Spätfolgen und die frühzeitige Erkennung möglicher Rezidive zu ermöglichen. Diese Nachsorge wird von einem multidisziplinären Team durchgeführt, das u.a. aus einem Allgemeinmediziner, einem Gynäkologen, einem Onkologen, einem Radiologen, einem Chirurgen, einem Ernährungsberater oder auch einem Psychologen besteht.
Das klassische Schema sieht Konsultationen alle drei bis vier Monate vor, dann fünf Jahre lang alle sechs Monate und anschließend einmal im Jahr. Dieser Überwachungsplan muss jedoch mit jedem Patienten besprochen und an ihn angepasst werden, insbesondere je nach Schwere der Krebserkrankung und dem Risiko eines Rückfalls. Bei Frauen, die an metastasierendem Brustkrebs erkrankt sind, erfolgt die medizinische Überwachung engmaschiger, nämlich alle zwei bis drei Monate oder alle zwei bis drei Chemotherapie-Sitzungen, wenn diese über einen längeren Zeitraum durchgeführt werden.
Die erste Mammographie zur Überwachung sollte ein Jahr nach der ersten Mammographie und mindestens sechs Monate nach Abschluss der Strahlentherapie durchgeführt werden.
Schließlich erfordert die Brustrekonstruktion alle ein bis zwei Jahre eine Nachuntersuchung mit dem Chirurgen, der sie durchgeführt hat.
Ein gesunder Lebensstil
Um das Fortschreiten der Krebserkrankung und die Nebenwirkungen der Behandlung besser bekämpfen zu können, ist eine abwechslungsreiche Ernährung mit entzündungshemmenden und antioxidativen Eigenschaften wichtig: Obst und Gemüse, Olivenöl, fetter Fisch, Nüsse, ... Wenn die Krebserkrankung mit einer Hormontherapie behandelt wird, können Vitamin-D- und Kalziumpräparate zur Vorbeugung von Osteoporose nützlich sein.
Eine regelmäßige körperliche Aktivität (Radfahren, Schwimmen, Spazierengehen, Gartenarbeit, Putzen usw.) ist ebenfalls wichtig. Es ist erwiesen, dass regelmäßige, mäßige und angepasste körperliche Aktivitäten helfen, die Müdigkeit nach der Behandlung zu bekämpfen.
Psychologische Unterstützung
Es ist wichtig, seine Zweifel und Ängste in Bezug auf die Krankheit (Auftreten neuer Nebenwirkungen, Fragen zu einer neuen Behandlung) mit seinem Arzt, aber auch mit seiner Umgebung zu teilen. Es ist auch von Vorteil, sich an Diskussionsgruppen und Vereinigungen von Patienten mit derselben Krankheit zu wenden. Sie können sich auch Teil von Online-Patientengemeinschaften wie dem Brustkrebsforum von Carenity werden. Falls nötig kann eine psychologische Betreuung (Psychologe, Psychiater, ...) in Betracht gezogen werden.
Wiederaufnahme der beruflichen Tätigkeit
Eine Arbeitsunterbrechung, deren Dauer von der Art der Behandlung und möglichen postoperativen Komplikationen abhängt, kann vom behandelnden Arzt verordnet werden. Darüber hinaus kann eine Anpassung für die Rückkehr an den Arbeitsplatz ins Auge gefasst werden, z.B. durch die Einführung einer therapeutischen Teilzeit für einen kurzen Zeitraum oder eine Anpassung des Arbeitsplatzes.
Zusammenfassend lässt sich sagen, dass Brustkrebs die häufigste Krebsart bei Frauen ist. Wenn er jedoch frühzeitig erkannt wird, kann er in 9 von 10 Fällen geheilt werden. Daher ist es wichtig, regelmäßige Selbstabtastung und Vorsorgeuntersuchungen durchzuführen. Darüber hinaus gibt es zahlreiche Behandlungsmöglichkeiten, die allein oder in Kombination eingesetzt werden. Sie werden an den jeweiligen Patienten (je nach seinen klinischen, biologischen und genetischen Merkmalen) angepasst und ermöglichen, trotz der Nebenwirkungen, eine Verbesserung der Lebensqualität und des Gesamtüberlebens der Patienten.
- Institut national du cancer: Le cancer du sein - points clés
- Ameli: Comprendre le cancer du sein
- Société canadienne du cancer: Qu’est-ce que le cancer du sein?
- Figaro santé: Cancer du sein
- Santé publique france: Cancer du sein
- HAS: Cancer du sein
- Vidal: Qu’est-ce que le cancer du sein?
- La ligue contre le cancer: Cancer du sein
- Fondation ARC: Cancers du sein: les traitements
- Fondation pour la recherche médicale: Comprendre le cancer du sein
- Universität München: Mammakarzinom
- Leben mit Brustkrebs: TNM-Klassifizierung und Stadieneinteilung
- Zentrum für Krebsregisterdaten: Brustkrebs
- MSD Manual: Überblick über Brusterkrankungen
Veröffentlicht am 17.01.2018 • Aktualisiert am 31.10.2021
Community Brustkrebs
Aufteilung der 520 Mitglieder auf Carenity
Altersdurchschnitt unserer Patienten
Infoblätter Krankheiten
Mehr



